老子道德經云:「道生一,一生二,二生三,三生萬物。」,而這個道,老子卻也語焉不詳,是言:「道可道,非常道。」。然而,科學家卻似乎不走這個思路,現代化學的不斷進展,從化合物、分子、原子、夸克等,不斷窮極所能地探尋,到目前為止,雖然仍無法全然參透老子的「道」(自然的法則),但如胡適先生所言:「近一寸有一寸的歡喜。」,經由近現代科學家鍥而不捨地研究,仍已得到卓然的成果。
而生物化學學家,則從蛋白質、RNA、DNA一直追溯,試圖解析萬物生長演變的法則。在他們的眼光中,基因就是了解這個「道」的一扇門,若能解析基因、編碼蛋白質、甚至其產物化合物的功能,就能了解生物體生長運作的原理。
什麼是天然物? 為什麼生物體要生產天然物?
天然物(Natural products)是由不同生物體,如植物、真菌、細菌等,所生產的有機化合物,通常具有生物活性或藥理活性,許多臨床上用來治療疾病的藥物,即是源自於天然物或是其衍生物。在人類的日常生活中,天然物也有著廣泛的應用,例如可作為香料、色素、染料、營養成分、植物荷爾蒙…等(圖一)。
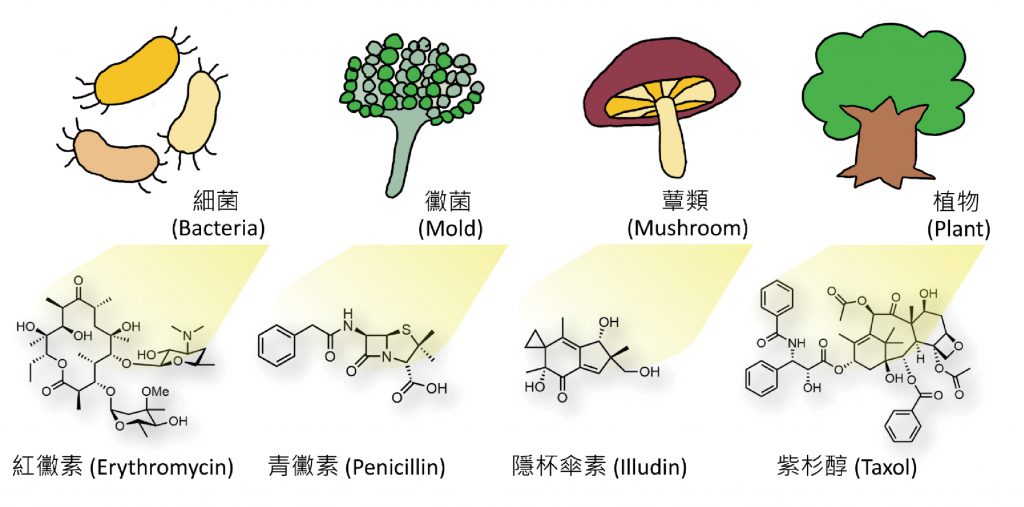
圖一、由各種生物體,如細菌、黴菌、蕈類、植物等,所生產的天然物例子。
天然物又可稱為二次代謝物(secondary metabolites),相較於對於生長不可或缺的一次代謝物,生物體如果缺乏生產二次代謝物的能力,並不會造成生物體的死亡,既然如此,為何生物體要生產天然物?
簡而言之,天然物的生產,可以為生物體提供演化上的優勢,有些天然物可在共生或寄生系統中,作為物種之間的訊息傳遞化學分子工具,例如赤黴菌(Gibberella fujikuroi)會生產一種萜類化合物‒gibberellin,為一種植物激素,可以促進植物生長和種子萌芽;而許多生物體所生產的天然物,具有細胞毒性,在不同物種之間.用來作為互相競爭、捕食、或自我防禦的分子武器。若我們能夠瞭解這些天然物的化學和生物活性之特性,則有機會在基礎研究或農業、醫藥上有廣泛的應用。
活性天然物的分離、化學結構鑑定以及醫藥應用
早期的天然物研究從十九世紀初期開始,從化合物的偵測、分離、純化至單一化合物、甚至結晶,舉例來說,在當時已經可以由金雞納樹的樹皮中萃取出奎寧(quinine)、從罌粟花分離出嗎啡(morphine)等成分,然而,仍尚無法確定化合物的結構。
1950年代X射線晶體學的開發,得以在分子層次解析天然物的化學結構。而大約從1960年代開始到二十一世紀初期間,核磁共振光譜儀以及質譜儀等方法的開發,大大地帶動了天然物的研究與發展,廣大數量的天然物化學結構,甚至其絕對立體構型,得以被發現以及精確地解析。
在這期間,天然物的化學結構,也啟發了許多化學家對於化學合成方法的建立和發展。同時,天然物的生物和藥理活性,也貢獻在醫藥應用上,核准當作臨床治療藥物的活性天然物,例如:用來治療瘧疾的青蒿素(artemisinin)、治療癌症的紫杉醇(taxol)、作為抗生素的青黴素(penicillin)和紅黴素(erythromycin)等(圖一)。
基因體時代—天然物是如何由生物體合成出來?
天然物在生物體內是如何被合成出來的?在早期主要使用化學方法,例如:同位素標定法,將標定的小分子前驅物經由生物體代謝後,利用標定原子在產物結構上之位置,推測其合成途徑。隨著基因體定序以及分子生物技術的進步,科學家得以從生物化學的角度,探討天然物的生物合成(biosynthesis)。
在生物體中,天然物的合成,可利用一次代謝物(primary metabolites)當作合成原料(圖二),或稱積木單元(building block),如同樂高組裝般地,建構成不同化學結構分子,而每一步驟的組裝都涉及不同化學反應,這些反應是由蛋白質(或稱酶、酵素,enzyme)所催化,經由多步驟化學反應進行天然物合成的方式,即稱為生物合成途徑(biosynthetic pathway)。
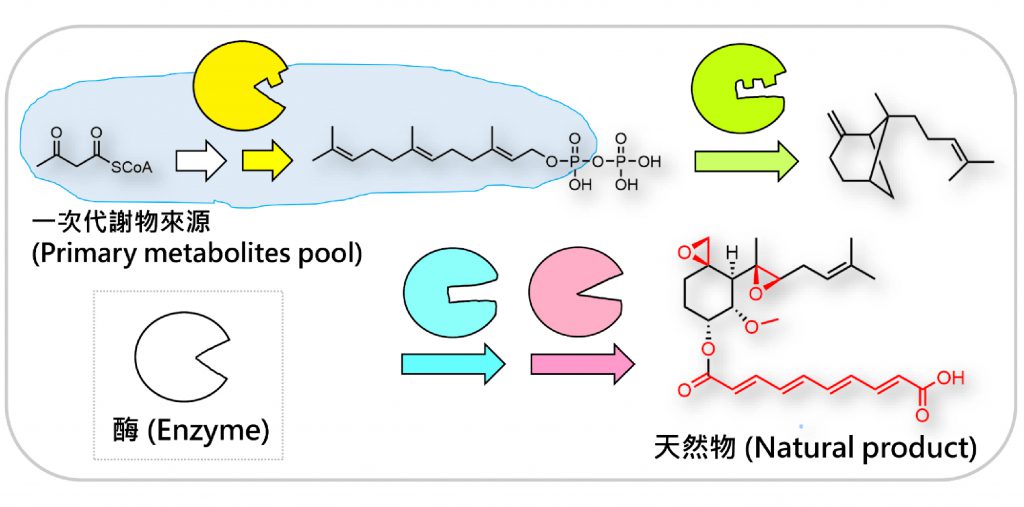
圖二、天然物的生物合成途徑。
有趣的是,在微生物,如細菌和真菌等,其基因體序列中,參與同一種天然物的生物合成途徑之相關基因,在染色體上的位置是群集的,稱為生物合成基因簇(biosynthetic gene clusters),由此透露著,一個生物體有多少生產天然物的能力,其實已編碼在它們的基因體中。
參與萜類天然物的生物合成途徑之氧化酶
萜類(terpenoids)是天然物的一大家族,常存在於我們日常生活中,例如各種揮發性香料如薄荷醇(menthol)、油畫用的松節油(turpentine),甚至臨床用藥,如青蒿素、紫杉醇等。萜類是由具有五個碳的isoprene單元(C5)所組成的天然物(C5n),從直鏈的isoprene diphosphate當作起始物,經由萜類環化酶(terpene cyclase)家族催化環化反應,形成多環的主結構(core scaffold),再由各種催化酶進行化學修飾,提供萜類的化學多樣性(圖三)。
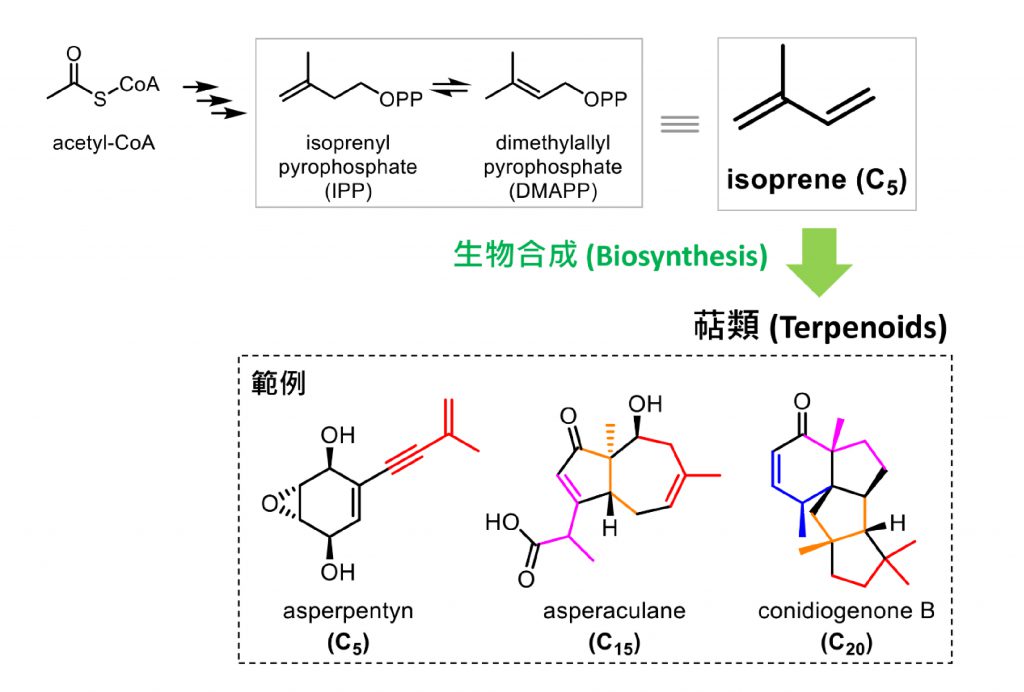
圖三、萜類天然物的生物合成,以isoprene為單元(C5),經由生物合成,組成化學骨架(C5n)以及結構修飾,形成的化合物稱為萜類天然物。在範例中的化合物,化學結構中衍生自isoprene單元的部分,分別以紅色、橘色、粉紅色、藍色表示。
萜類天然物的生物合成途徑中,常伴隨著氧化反應所參與的碳‒氫鍵活化(C‒H functionalization),一種將碳氫鍵切斷而形成碳‒碳、碳‒氧、或碳‒氮等鍵結的反應。碳‒氫鍵的鍵能高,不容易產生反應,因此,如何在溫和條件下,高度選擇性地進行碳‒氫鍵活化,具有其挑戰性以及應用性。
我們近年來研究萜類天然物的生物合成途徑,發現了幾種由P450氧化酶(P450 monoxygenases)所催化的化學反應,涉及特別的碳‒氫鍵活化。在其中一個研究中,與中研院化學所陳榮傑老師合作,我們報導一個特別的P450氧化酶AtyI,可催化多步驟氧化反應,將isoprene單元的衍生基團轉化成具有1,3-烯缺官能基。
P450氧化酶AtyI催化雙重氧化反應,將異戊二烯基轉成1,3-烯炔
烯炔官能基在有機合成、材料和藥物化學有著廣泛應用,為有機化學的重要官能基之一,目前已有許多化學合成方法可合成烯炔,然而,對於自然界中生物體如何催化烯炔的形成,仍了解甚少。我們觀察到在一些天然物的化學結構中,具有烯炔官能基,這意味著在自然界存在著未知的催化酶,可以將化合物安裝上這種化學基團。
有一種自土壤分離的真菌Aspergillus sp. PSU-RSPG185,曾被報導會生產具有烯炔的asperpentyn天然物(圖四),它的結構極為簡單,但其生物合成途徑和參與酶是未知的。首先,我們定序了這株真菌的基因體序列,進行生物資訊分析,尋找可能的asperpentyn生物合成基因簇,我們發現了一個基因簇(稱為aty) (圖四a),它的編碼基因功能,可能與我們推測的asperpentyn生物合成途徑中,所參與的化學反應相關,除此之外,此基因簇也存在於其他會生產烯炔天然物的真菌基因體中。
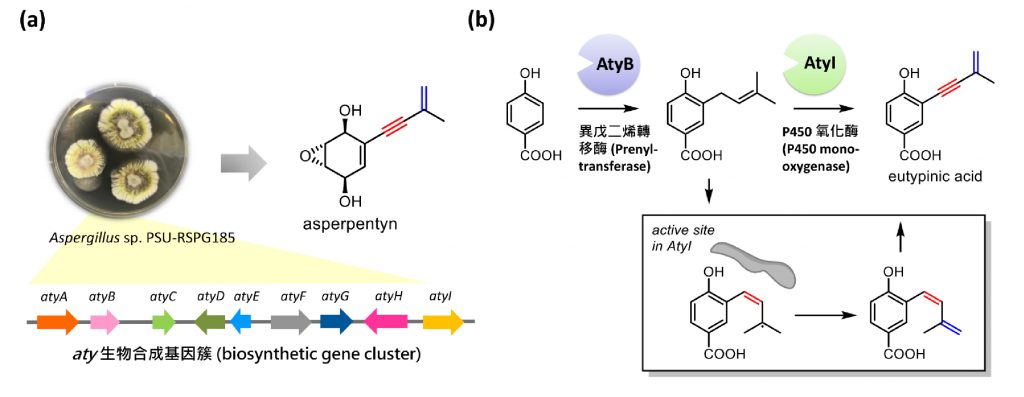
圖四、(a) 萜類天然物—asperpentyn,在真菌Aspergillus sp. PSU-RSPG185的生物合成基因簇;(b) P450氧化酶AtyI的催化功能,可將異戊二烯取代基進行脫氫反應,形成順式二烯中間體,接下來具有炔酶功能,催化1,3-烯炔的形成。
我們利用釀酒酵母菌(Saccharomyces cerevisiae)異源表達系統(heterologous expression),表達aty基因簇上的編碼基因,並利用餵養實驗、細胞外的酶反應實驗,確認編碼蛋白的功能。這個研究發現了一個獨特的P450氧化酶AtyI,該酶具有雙重催化功能,首先,催化異戊二烯鏈的脫氫反應,形成順式二烯中間體,接著具有炔酶功能,進而生產炔烴,得到1,3-烯炔(圖四b)。除此之外,利用有機化學方法所製備的一系列受質衍生物以及中間體類似物,解析AtyI合成烯炔的催化機制,發現AtyI必須辨認順式烯基,即可發揮炔酶功能。此研究提供了一個新穎合成方式—利用酶工具合成1,3-烯缺官能基[1]。
破解生物合成途徑的基因密碼,在現今的應用
了解基因編碼蛋白的功能,科學家們可以利用基因工程的方式,設計基因表達迴路,調整各迴路的表達量,或是生物合成途徑上游的原料補給,在適當的基因表達細胞工廠(如細菌、酵母菌、甚至是植物等),達成高效率的化合物生產。近年來有幾個代表性的例子,如植物天然物—青蒿素[2]、嗎啡(morphine)[3]和大麻酚(cannabinoids)[4],其生物合成途徑可以在酵母菌成功建立並生產化合物。
另一方面,特別的酶功能之發現,有機會開發生物催化劑(biocatalysts),應用在工業製程。代表例子如,醯基轉移酶(acyltransferase) LovD,經由優化其對特定受質的催化能力,已應用於降血脂藥物simvastatin的製成,此方法可減少能源以及大量化學試劑的使用,因此取代了原本利用化學試劑合成之製程方法[5]。
大航海時代—尚待發掘的催化酶寶藏
根據分子生物學的中心信條(The Central Dogma,或稱核酸控制蛋白法則),將基因體序列進行分析,科學家能夠推測一個生物體能夠表達的蛋白質家族和類型之潛力。儘管已有許多天然物生物合成途徑以及其參與基因之功能被解析,但仍無法準確地由基因序列預測,其相對應的生物合成途徑,以及生產化合物為何。在一個對581個真菌基因體序列的分析研究中指出,僅有約3%數目的生物合成基因簇,是已由研究驗證其功能,然而仍有約97%數目的生物合成基因簇,其功能仍是尚待發掘[6]。
面對這些尚未了解功能的基因和酶,科學家利用許多不同方法與策略進行探索,期能找到新穎的催化酶寶藏,了解與其相關的天然物生物合成。各種新穎酶化學催化功能的發現,將有助於利用生物方法,了解大自然使用的化學工具。
Reference:
[1] Angew. Chem. Int. Ed., 2020, 59, 13537 –13541
[2] Nature, 2013, 496, 528–532
[3] Science, 2015, 349, 1095–1100
[4] Nature, 2019, 567, 123–126
[5] https://www.epa.gov/greenchemistry/presidential-green-chemistry-challenge-2012-greener-synthetic-pathways-award
[6] Fungal Genet. Biol., 2016, 89, 18–28
